접수방법
심의종류별 제출서류를 구비하여 의약품 임상시험의 경우는 원본 1부, 사본 10부, 의료기기 임상시험의 경우 원본 1부, 사본 10부를 제출해야 되며, 목차 별로 구분이 가능하도록 Tag를 삽입하여 주시기 바랍니다. CD에는 원본의 내용이 들어있는 PDF파일을 제출해야 되며, PDF파일로 제출이 어려운 경우 *.doc, *.hwp 등 작성하신 형식의 파일로 제출하여도 무방합니다. PDF파일의 파일명은 제출서류의 목차명과 동일하게 국문으로 작성하여 주시기 바랍니다.
심의종류별 제출서류
의약품 임상시험
- 최초심사의뢰
- 연구계획 심사의뢰 시 제출 서류, 양식 SJIRB19-001(부록 1)
- 임상시험계획심사의뢰서
- 연구계획서 목차, SJIRB19-002(부록 2)
- 연구계획서(요약)
- 보완된 연구계획서 재심사
- 시정승인에 대한 답변
- 검토의견에 대한 답변서
- 해당 시정항목에 관련한 서류
- 보완 후 재심사에 대한 답변
- 연구계획 심사의뢰시 제출 서류, 양식 SJIRB19-001 (부록 1)
- 임상시험계획심사의뢰서
- 연구계획서 목차 SJIRB19-002(부록 2)
- 연구계획서(요약)
- 임상시험 중대한 이상반응 보고서
- 중대한 이상반응보고서
- 타기관 중대한 이상반응보고서
- 연구계획변경
- 접수된 안건 체크리스트, 양식 SJIRB 08-001
- 문서접수양식
- 임상시험 계획변경신청서
- 승인된 연구계획서의 지속심사
- 접수된 안건 체크리스트 양식
- 문서접수양식
- 지속심사 신청양식, SJIRB 09-001
- 연구종료
- 접수된 안건 체크리스트 양식
- 임상시험 종료보고서
- 임상시험 최종결과
의료기기 임상시험
- 최초심사의뢰
- 연구계획 심사의뢰시 제출 서류 (SJIRB19-001 참조)
- 임상시험계획심사의뢰서 (SJIRB 05-001 참조)
- 연구계획서 목차 (SJIRB19-002참조)
- 연구계획서(요약 및 작성요령); (SJIRB19-003, 004참조)
- 추가적으로 제출을 요구할 수 있는 서류
- 의료기기 등급 분류와 그에 따른 품목 정보
- 이해상충과 관련한 서약서, (SJIRB 19-015 참조)
- 의료기기 임상시험 점검표, (SJIRB 05-002 참조)
- 시험자 준수 서약서, (SJIRB 19-016 참조)
- 보완된 연구계획서 재심사 의뢰
- 시정승인에 대한 답변
- 검토의견에 대한 답변서, (SJIRB 19-014 참조)
- 해당 시정항목에 관련한 변경 서류
- 보완 후 재심사에 대한 답변
- 연구계획 심사의뢰 시 제출 서류, (SJIRB19-001 참조)
- 임상시험계획심사의뢰서, (SJIRB 05-001 참조)
- 연구계획서 목차, (SJIRB19-002참조)
- 연구계획서(요약) , (SJIRB19-003, 004참조)
- 바뀌기 전과 바뀐 후의 내용과 사유를 담은 변경대비표
- 변경된 서류
- 임상시험 중대한 이상반응 보고
- 중대한 이상반응 보고서, (SJIRB 10-001 참조)
- 타기관 중대한 이상반응 보고서, (SJIRB 10-002 참조)
- 임상시험 계획변경
- 임상시험 계획 변경 신청서 (SJIRB 08-001 참조)
- 바뀌기 전과 바뀐 후의 내용과 사유를 담은 변경대비표
- 변경된 서류
- 승인된 연구계획서의 중간/지속심사 보고
- 임상시험 중간/지속심사 보고서(SJIRB 09-001)
- 임상시험의 진행사항을 요약 기술한 중간보고
- 임상시험 과제점검리스트 (SJIRB 09-002)
- 그 밖의 심사에 필요한 서류
- 임상시험 조기종료/일시중지 보고
- 임상시험 조기종료/일시중지 보고서 (SJIRB 12-001)
- 중지 또는 조기 종료하는 사유
- 그 동안의 임상시험 진행사항을 요약 기술한 내용
- 연구종료 / 최종결과 보고서 심사
- 임상시험 종료 보고서 (SJIRB 13-001 참조)
- 임상시험 최종결과 보고서 (SJIRB 13-002 참조)
- 중지 또는 조기 종료하는 사유
- 그 동안의 임상시험 진행사항을 요약 기술한 내용
- 연구비 사용내역(해당되는 경우) (SJIRB 19-013 참조)
심사비
심사비 목록 - 구분, 심의종류, 금액, 비고 정보 제공
| 구분 |
심의종류 |
금액 |
비고 |
| 국책과제 연구비(연구비에서 충당 가능한 경우) |
초기심의 |
600,000원 |
|
| 지속심의 |
400,000원 |
지속심의 주기와 관련 없이 년 1회 산정 |
| 스폰서 임상시험연구(SIT) & PMS |
초기심의 |
600,000 ~ 800,000원 |
연구비 비례 : 5천만 원 이상 80만원, 5천만 원 이하 60만원 |
| 지속심의 |
400,000원 |
지속심의 주기와 관련 없이 년 1회 산정 |
| 연구자 임상시험연구(IIT) & PMS |
초기심의 |
200,000원 |
단, 병원 및 상지대 교원 50%할인. 지속심의 주기와 관련 없이 년 1회 산정 |
| 지속심의 |
200,000원 |
| 신속승인 가능한 연구(사회과학계열 및 기타연구) |
초기심의 |
100,000원 |
단, 병원 및 상지대 교원 50%할인. 지속심의 주기와 관련 없이 년 1회 산정 |
| 지속심의 |
100,000원 |
| 면제가능 연구 |
초기심의(신속) |
80,000원 |
단, 병원 및 상지대 교원 50%할인. 면제가능 사항 참조 |
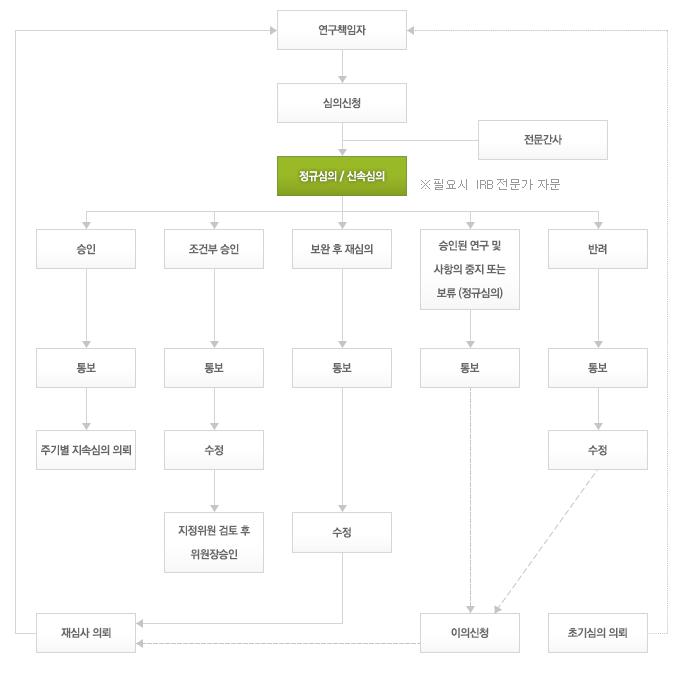
심의흐름도